Protein kolajen parçaları 80 milyon ila 195 milyon yıllık dinozor fosillerinde korunmuş olarak bulunmuştur. Ama bu mümkün olmamalıydı. Proteinleri bir arada tutan peptit bağlarının, sadece 500 yıllık bir yarılanma ömrü ile çok çok daha erken parçalanması gerekir.
Şimdi, ACS Central Science'da yapılan yeni bir çalışma, kolajenin olağanüstü uzun ömürlülüğünden sorumlu koruyucu kimyayı tanımladı.
Hayvanlarda en bol bulunan protein olan kolajen kemiklerde, deride, kaslarda ve bağlarda bulunur.
Çalışmanın kıdemli yazarı, ABD'deki Massachusetts Teknoloji Enstitüsü'nde (MIT) kimya profesörü olan Ron Raines, kolajenin bizi bir arada tutan iskele olduğunu söylüyor.
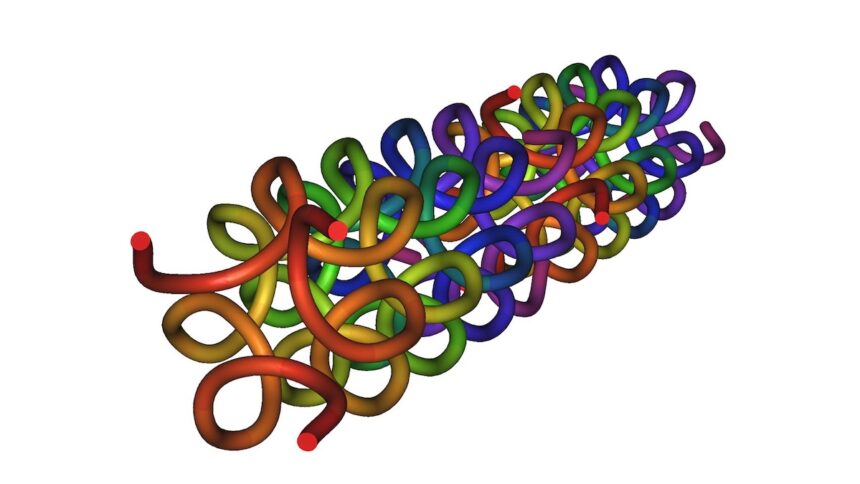
Raines, "Kolajen proteinini bu kadar kararlı ve bu iskele için bu kadar iyi bir seçim yapan şey, çoğu proteinin aksine lifli olmasıdır" diyor.
Üçlü sarmal bir yapı oluşturmak için ip gibi iç içe geçen uzun amino asit ipliklerinden oluşuyor. Kolajenin peptit bağlarına su ile parçalanmaya (hidroliz) karşı benzersiz direnç kazandıran da bu yapıdır.
Bir proteindeki ardışık amino asitleri birbirine bağlayan peptit bağları, bir amino asitteki bir karbon atomu ile bitişik amino asitteki bir nitrojen atomu arasında oluşur.
Karbon atomu ayrıca bir oksijen atomu ile çift bağ oluşturarak karbonil grubu olarak bilinen moleküler bir yapı meydana getirir.
Bu karbonil oksijen, başka hiçbir atomla bağ oluşturmayan bir çift elektrona sahiptir. Araştırmacılar, bu elektronların komşu bir peptit bağının karbonil grubuyla paylaşılabileceğini buldu.
Bu etkileşimler kolajen üçlü sarmalındaki hemen hemen her peptit bağını birbirine bağladığından, normalde bu bağları hidroliz yoluyla bozmak için yapıya girecek olan su moleküllerini engeller.
Raines, "Kolajen bir uçtan diğer uca üçlü sarmaldan oluşuyor," diyor. "Zayıf bir halkası yok ve bence bu yüzden hayatta kalmayı başardı."
Araştırmacılar, bu etkileşimlerden çıkarılan derslerin diğer olağanüstü kararlı, uzun ömürlü malzemelerin tasarımına rehberlik edebileceğini söylüyor.