Les essais cliniques sont nécessaires pour évaluer l'efficacité et la sécurité des médicaments sur des sujets humains. Bien que l'objectif général de la recherche biomédicale soit d'améliorer la santé et le bien-être de l'ensemble de la population, les participants aux essais cliniques ont tendance à manquer de diversité. Une analyse portant sur 32 000 personnes ayant participé à des essais de nouveaux médicaments aux États-Unis en 2020 a révélé que seulement 8 % des participants étaient noirs, 6 % étaient asiatiques, 11 % étaient hispaniques et 30 % avaient 65 ans ou plus.
Une nouvelle revue menée par Simon Groen, professeur adjoint en biologie des systèmes évolutifs à l'Institute for Integrative Genome Biology de l'Université de Californie à Riverside, et Sophie Zaaijer, consultante et chercheuse spécialisée dans la diversité, l'équité et l'inclusion (DEI) dans les recherches cliniques à UC Riverside, a exploré comment un aspect de la race – le teint de la peau – influence l'efficacité des médicaments.
"Notre article de revue conclut que la mélanine, le pigment responsable de la couleur de la peau, montre une affinité surprenante pour certains composés médicamenteux", a déclaré Groen. "Les effets de la mélanine sur la sécurité et le dosage des médicaments ont été largement ignorés, et comme les gens varient considérablement en termes de teint de peau, des questions préoccupantes se posent quant à l'efficacité des dosages standard."
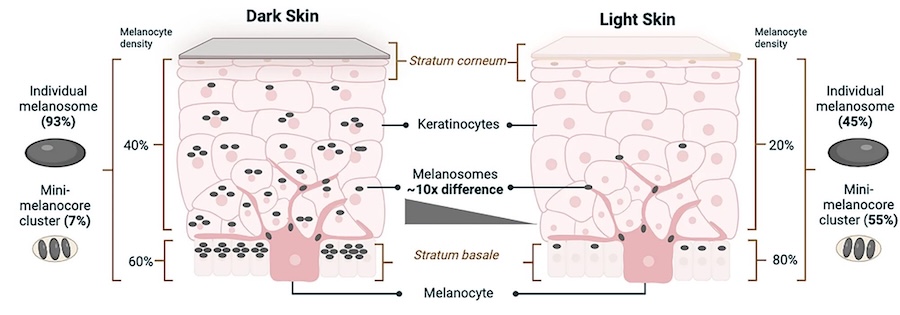
Les cellules clés du teint de la peau humaine sont les mélanocytes, qui produisent les mélanosomes contenant de la mélanine, et les kératinocytes, qui les stockent. Le nombre et les caractéristiques des mélanosomes dans les couches de la peau déterminent les variations de teint, du clair au foncé. La peau foncée contient un taux plus élevé de mélanosomes individuels de grande taille, tandis que la peau claire contient des niveaux plus élevés de grappes de mini-mélanosomes. Dans la peau claire, les mélanosomes sont concentrés dans la couche la plus profonde de la peau, le stratum basale, tandis que dans la peau foncée, ils sont dispersés de manière plus diffuse à travers les couches.
La combinaison unique des deux principales formes de mélanine (phéomélanine et eumélanine) chez une personne est responsable de la couleur de la peau, des cheveux et des yeux. L'eumélanine, en raison de sa structure chimique, offre une affinité élevée pour se lier à diverses substances, y compris les médicaments basiques ou neutres et les ions métalliques, jouant ainsi un rôle important dans les interactions médicamenteuses. Parmi les composés ayant une affinité de liaison avec l'eumélanine, on trouve la cocaïne, la nicotine, l'analgésique acétaminophène, les antibiotiques ampicilline, ciprofloxacine et pénicilline G, les antidépresseurs clomipramine et imipramine, ainsi que les antipsychotiques chlorpromazine, clozapine et halopéridol.
Prenons l'exemple de la clozapine, un antipsychotique : c'est le seul médicament approuvé par la FDA pour le traitement de la schizophrénie résistante. Une étude de 2023 a utilisé une étude d'association pangénomique (GWAS) pour examiner le métabolisme de la clozapine parmi et entre différentes ascendances : européenne, subsaharienne, nord-africaine, sud-ouest asiatique et est-asiatique. À dose égale, il a été constaté que l'ascendance subsaharienne était associée à des concentrations plasmatiques de clozapine plus faibles que l'ascendance européenne.
Bien que la peau soit le plus grand organe du corps, elle a été largement négligée en ce qui concerne les interactions potentielles entre l'eumélanine et la pharmacocinétique (ce que le corps fait au médicament ; comment le médicament entre et sort du corps) et la pharmacodynamique (ce que le médicament fait au corps ; les effets biochimiques, physiologiques et moléculaires du médicament). Des études ont montré que les variations des niveaux d'eumélanine dans la peau – et donc du teint – pourraient influencer l'utilisation et la dépendance à la nicotine, ce qui a des implications pour les personnes à la peau plus foncée utilisant des patchs de nicotine comme aide au sevrage tabagique.
Groen a demandé : "Si les fumeurs à la peau foncée utilisent ces patchs dans leurs tentatives d'arrêter de fumer, les sous-dosons-nous involontairement ?"
Les chercheurs soutiennent que les directives actuelles pour les essais cliniques ne prennent pas suffisamment en compte l'impact de la pigmentation de la peau sur les interactions médicamenteuses.
Zaaijer a déclaré : "Comme indiqué dans le Plan d'action pour la diversité de la FDA, cette négligence est particulièrement préoccupante compte tenu de la pression pour des essais cliniques plus diversifiés. Cependant, les pratiques actuelles de développement de médicaments en phase précoce se concentrent toujours principalement sur des tests de médicaments dans des populations blanches d'origine nord-européenne."
Conformément aux dispositions récemment entrées en vigueur de la Loi sur la réforme multifonctionnelle des aliments et des médicaments (FDORA), la FDA exige que les sponsors d'essais cliniques de phase 3 ou d'"autres études importantes sur un médicament" soumettent un Plan d'action pour la diversité conçu pour augmenter l'inscription de participants provenant de populations historiquement sous-représentées. Un "sponsor" est défini comme la personne, la société pharmaceutique, l'institution académique, l'organisation privée ou autre entité qui assume la responsabilité d'une étude clinique et la lance.
Zaaijer a ajouté : "La FDA a récemment publié ses projets de lignes directrices. Une fois finalisées dans quelques mois, elles rendront obligatoire la prise en compte de la diversité des patients dans les études cliniques et dans la R&D préclinique [recherche et développement]. La prochaine étape consiste à fournir des orientations sur les variables pharmacocinétiques à tester dans les pipelines de R&D pharmaceutique dans la quête de médicaments équitables."
C'est un pas dans la bonne direction, mais le changement prendra un certain temps.
Zaaijer a expliqué : "En termes de tests de profil de risque, les médicaments sont principalement testés sur un ou plusieurs modèles de cellules humaines provenant de donneurs d'origine nord-européenne. Les médicaments sont ensuite testés sur un modèle de rongeur. Si ces tests réussissent, les sociétés pharmaceutiques passent aux essais cliniques. Mais si les médicaments n'ont pas été testés, par exemple, sur des modèles de cellules humaines de différentes ascendances, sont-ils prêts à être administrés à divers groupes de patients ? Feriez-vous du saut à l'élastique d'un pont si vous saviez que les cordes n'ont pas été testées pour votre catégorie de poids ? Probablement pas. Alors pourquoi est-ce acceptable pour les médicaments ?"
Groen et Zaaijer proposent comme solution que les sociétés pharmaceutiques utilisent des modèles de peau humaine 3D de différentes pigmentation pour évaluer les propriétés de liaison des nouveaux médicaments.
Zaaijer a déclaré : "La pigmentation de la peau doit être prise en compte comme un facteur dans les estimations de sécurité et de dosage. Dans l'industrie biomédicale, nous sommes au seuil d'une ère transformative où l'adoption de l'inclusivité n'est plus une option, mais une nécessité."
Les chercheurs encouragent également les patients et les participants aux essais cliniques à poser des questions telles que : "Ce médicament a-t-il été testé pour voir s'il est sûr pour des personnes d'ascendances différentes comme la mienne ?"
Groen a conclu : "Si les différentes ascendances sont prises en compte dès les premières étapes de la découverte de médicaments, divers groupes de personnes pourraient avoir plus confiance dans le processus de développement des médicaments et s'inscrire aux essais cliniques, car ils seraient mieux informés des risques potentiels associés."
L'article a été publié dans la revue Human Genomics.




